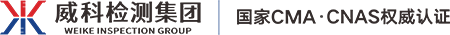体外膜氧合(ECMO)循环套包动物试验注册审查指导原则
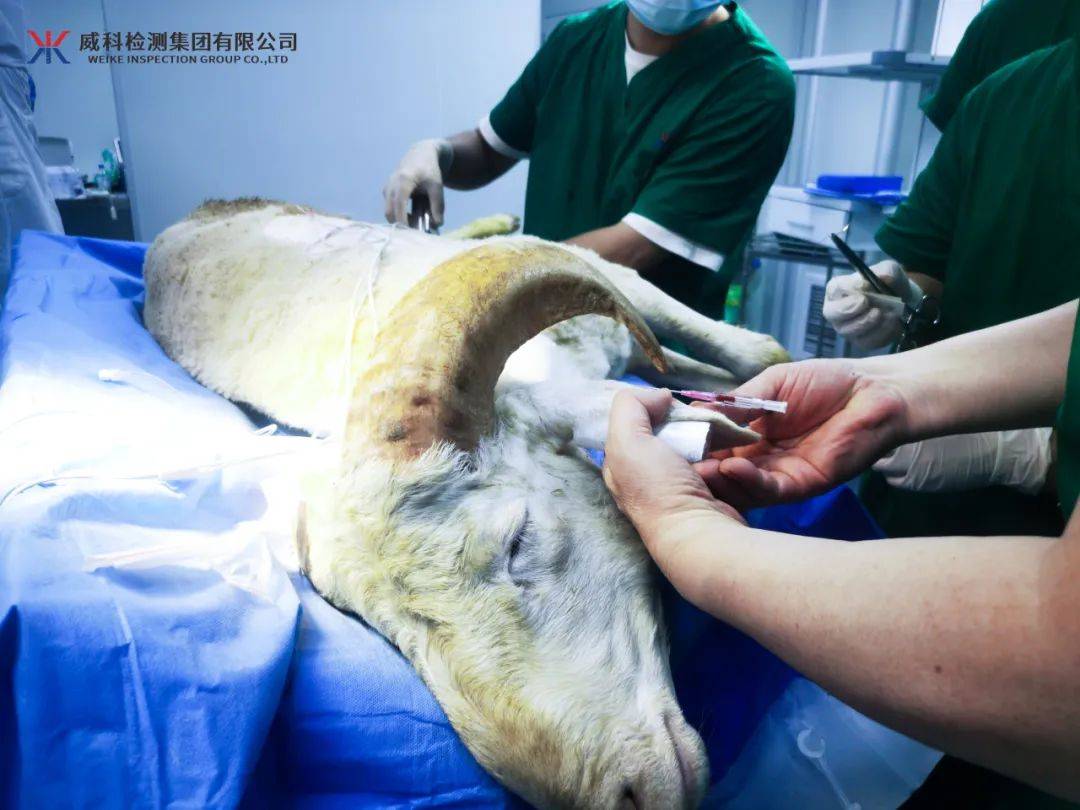
体外膜氧合(ECMO)是体外生命支持(ECLS)技术的一种,用于部分或完全替代患者心肺功能,使其得以充分休息,从而为原发病的诊治争取时间。考虑到ECMO是一项成本高昂、技术复杂、并发症较多的生命支持技术,以及由于台架试验的局限性,开展ECMO产品的动物试验有重要的意义,一方面可在产品开发环节中为产品设计定型提供相应的证据支持,另一方面可在临床试验前为医疗器械能否用于人体研究提供支持信息,为临床试验设计提供参考。
为了进一步规范体外膜氧合(ECMO)循环套包产品动物试验,并指导该类产品申请人在申请产品注册时动物试验资料的准备,制定本指导原则。
本指导原则系对ECMO循环套包产品动物试验的一般要求,注册申请人需依据具体产品的特性对注册申报资料的内容进行充实和细化,并确定其中的具体内容是否适用。
本指导原则是对注册申请人和审评人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不强制执行,如果有能够满足相关法规要求且更为科学的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。需在遵循相关法规和标准的前提下使用本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制订的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时的调整。
本指导原则适用于体外膜氧合(ECMO)循环套包和膜式氧合器产品,套包一般包括膜式氧合器、离心泵泵头、体外循环管路和体外循环插管等组件。
对于其他形式的套包组合或单独申报的特定组件产品,申请人可参照《医疗器械动物试验研究技术审查指导原则 第一部分:决策原则》及本指导原则,并根据申报产品适用情况参考使用。
本指导原则不适用于心肺转流系统最多持续使用6小时的膜式氧合器及附件。

动物试验的考虑因素
(一)试验目的
ECMO技术通过引流患者静脉血至体外,经过氧合和二氧化碳清除后回输患者体内,承担气体交换和(或)血液循环功能,能够对急性呼吸和/或循环衰竭患者进行全部或部分心肺支持。根据治疗方式和目的不同,ECMO 技术主要有静脉到静脉(veno-venous ECMO,VV-ECMO)和静脉到动脉(veno-arterial ECMO,VA-ECMO)两种形式,前者仅具有呼吸辅助作用,后者同时具有循环和呼吸辅助作用。
对该类产品的动物试验研究,申请人首先应对申报产品进行风险分析,充分考虑产品已知或潜在风险。
动物试验研究根据目的一般分为可行性研究、安全性研究和有效性研究,但有时不能严格划分界限,在一项动物试验中可同时对产品的可行性、有效性、安全性进行评价。
在安全性方面,考虑到ECMO是一项技术复杂和并发症较多的生命支持技术,ECMO产品的性能和(或)有效性与其安全性密切相关,因此,考察和评价ECMO产品的安全性是产品综合评价中的重要部分。基于目前ECMO技术的临床使用经验,建议在动物试验中根据申报产品适用情况对已发现的ECMO技术对健康的主要风险予以评价。
例如:
*血小板减少症:使用ECMO产品可能会对血小板产生损害,血小板减少可能导致出血倾向。
*溶血:红细胞可能会因体外循环的机械作用、剪切力、材料或表面特征而受损。
*组织不良反应:某些情况下,接触患者的材料可能在患者体内引起不良免疫学反应(如过敏反应、炎症反应)。
*出血:为了防止体外循环回路凝血,ECMO治疗中通常会使用抗凝剂,这可能会在治疗期间增加患者出血风险。
*血液稀释:ECMO体外循环回路的预充可能导致患者血液稀释。
*血栓形成:由于血流流速过低,血液滞留或抗凝不充分,可能会在体外循环回路内形成血栓。
*感染:产品设计或结构缺陷会导致无法充分进行清洁和/或灭菌,从而可能引入病原体并可能导致感染。
*血管机械损伤:ECMO产品对血管的机械损伤可能是插管时的急性损伤,也可以是长期使用过程中,随着时间推移出现的慢性损伤。
*气体栓塞:体外循环回路可能会引入空气并导致气体栓塞。
*机械故障:在ECMO产品的预期使用期限内,产品设计缺陷、机械完整性问题、回路组件连接或结构方面的不足可能导致循环回路破裂(泄漏)、性能故障、渗血等。
在有效性方面,建议根据申报产品的性能特征等因素进行有效性评价,例如,可考虑氧合器的气体交换性能(氧合器的设计缺陷或机械故障可能导致气体交换能力改变)、热交换性能(如适用)、离心泵流体动力学性能等。对于需验证申报产品在某些功能上的特殊优势时,可考虑与此相关的有效性评价。除申报产品的有效性评价外,建议对其他组件性能是否满足使用要求亦进行记录。
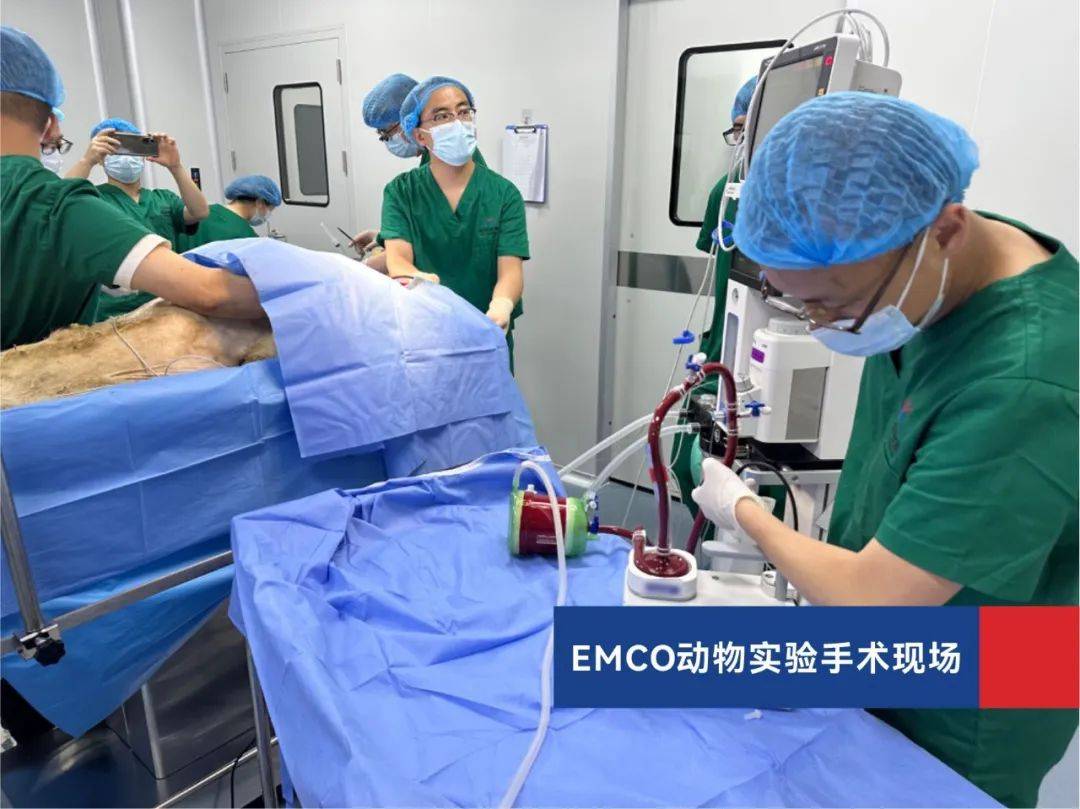
实验用动物种类及模型
选择适用的实验动物进行ECMO产品的动物试验研究是获得可靠、科学证据的基础,申请人需对动物试验中所采用实验动物的适用性进行分析,提供实验动物种类选择及模型建立的确定依据,如文献资料、同类产品的动物试验证据等信息。一般而言,羊、猪、牛等比较大型且相对温顺的动物由于其以下优势,比较适宜进行相关研究:
(1)羊、猪等大型哺乳动物的解剖学、生理学与人体类似,ECMO治疗时设备的放置方式(如插管位置)及相关参数设定与在人体内使用时类似,同时可对其使用标准的临床重症监护设备,更好地模拟ECMO产品的临床使用环境,便于收集循环监测数据。动物模型较大,也便于获取足够的组织样本以进行必要的研究分析;
(2)羊、猪等动物模型已广泛用于心血管系统产品的研究,在动物管理方面已有较多的经验;
(3)与猪相比,羊是相对更加温顺的动物,适用于验证ECMO长期应用性能的动物试验。
是否采用疾病模型可根据动物试验拟验证的风险及研究目的进行确定,但考虑到某些疾病模型动物存活时间较短、疾病模型的偏倚等因素,如需验证ECMO长期应用性能,可考虑采用健康动物进行试验。选择健康动物的试验时,需在试验前(如手术操作前)对动物健康状态进行评价,保证其体格检查、血液检测指标(如血常规、血生化检测)等在临床可接受的正常范围内。对于选择特定疾病模型动物的试验,需评价动物建模是否成功。考虑到ECMO支持产品可能针对不同的适用人群,如小儿患者,在选择动物时可以考虑采用相似心输出量及血流量范围幼龄动物。
动物性别、规格(如年龄和体重)、健康和疾病状态、病原体感染情况等均可能会对动物试验结果和结论造成影响,因此试验用动物选择时宜充分考虑上述因素。
对照的选择
申请人应对是否设立对照组进行分析论证。例如需验证申报产品在某些功能指标上的特殊优势,或验证与同品种产品对比等情况,可设立对照组。
若需设立对照组,建议申请人根据评价指标特点等选择对照器械和/或对照材料、对照支持模式等。宜优先选择已上市的同类器械作为对照并考虑随机化的设计并予以描述。
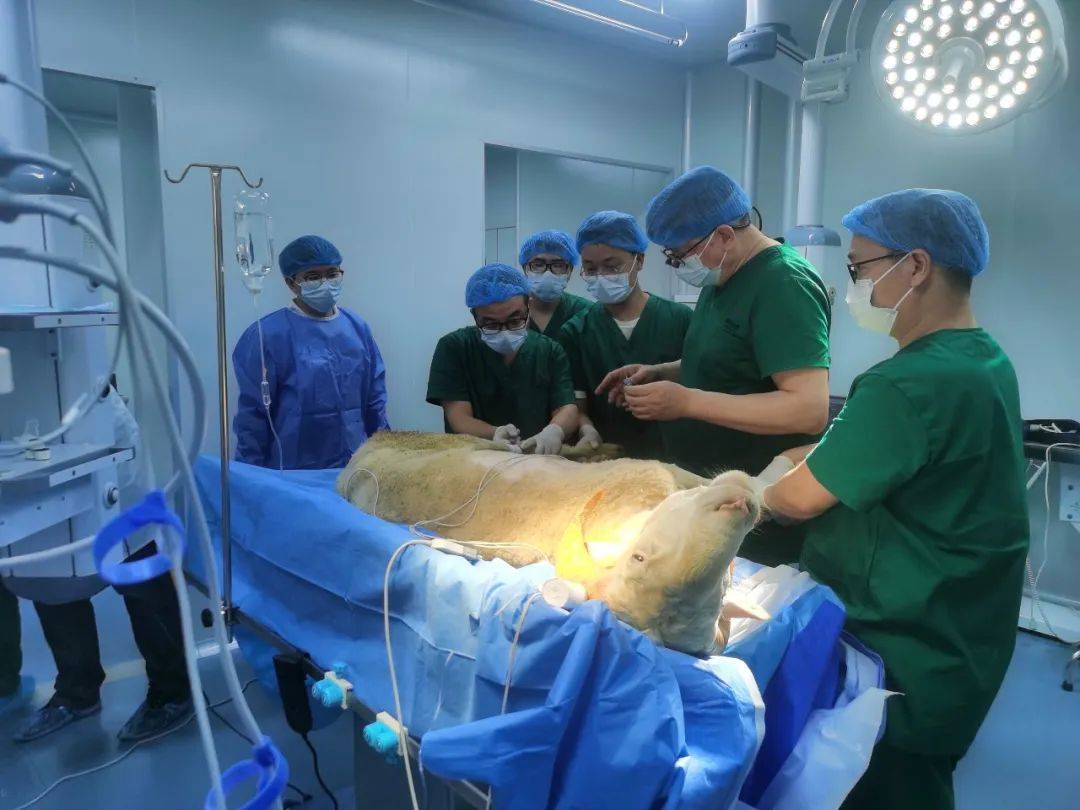
评价指标的选择
在选择评价指标时,建议综合考虑试验目的、产品特征等因素,制定科学、客观的评价标准。需明确具体评价指标的观察时间点和频次。同时,需根据试验目的确定主要指标和次要指标,并对评价标准进行说明。例如,对于氧合器产品性能评价的动物试验,主要有效性评价指标可选择产品达标率,其中产品达标需满足氧合性能,如通过氧合器后的氧分压和二氧化碳分压等达到评价标准要求。
通常情况下,ECMO产品的动物试验中建议包括(但不限于)以下指标:
1.血液相关的实验室检查指标:血常规(白细胞计数、红细胞计数、血小板计数、血红蛋白、红细胞压积)、血生化(总蛋白、白蛋白、球蛋白、ALT、AST、胆红素、肌酐、尿素氮)、血浆游离血红蛋白、C反应蛋白、凝血(ACT、APTT、纤维蛋白原、纤维蛋白原降解产物、血浆-D二聚体)、血气(乳酸、氧分压、二氧化碳分压、氧饱和度、pH)等。
2.病理学相关指标:1)大体病理学:对试验动物进行尸检时,需提供主要器官的原位照片,同时关注插管血管是否有机械损伤、主要动静脉(如股静脉/动脉、颈静脉/动脉)中是否有血栓形成、脏器(脑部、肝脏、肾脏、脾脏、肠道、心脏和肺部)是否可见梗死或出血灶等。尸检时发现的任何潜在血栓建议均进行组织病理学检查。2)采集肺、心、肝、肾和脑组织标本进行组织病理学检查。
3.生命体征及血流动力学监测:血压(可考虑有创血压监测,获得动脉压、中心静脉压等)、心率、体温、呼吸频率。
4.ECMO运行期间监测并记录血流量、气体流量、氧合器的跨膜压差及气体交换性能(O2输送和CO2清除)等主要治疗参数,观察器械外观变化,监测可能的器械故障(如泄漏)。对于组件更换需进行记录和原因分析。
5.定期查看实验动物插管部位是否有机械损伤和感染迹象。
6.动物试验中,宜对任何安全性事件/异常进行记录和分析。如果发生动物死亡,应详细分析死亡的原因,分析同产品相关性。
7.实验动物尸检时,应同时观察器械外观变化,可考虑对产品进行剖开检查,关注是否有血栓、赘生物、梗死灶。也可以对回收器械进行体外性能检测。
若需验证申报产品的某些特殊功能和/或性能时,可选择针对相关功能和/或性能的特定评价指标,同时提供相关评价指标的确定依据。
观察时间点的选择
制定动物试验观察时间时需考虑选择的动物模型种类、产品预期使用时长、试验目的等因素,并提供合理的确定依据。对于需验证产品长期使用可靠性和耐久性的试验,考虑到过长时间的ECMO治疗会导致实验动物并发症明显增加(如血栓相关并发症),观察时间应考虑一定冗余。例如,对于氧合器产品,动物试验观察时间可考虑为临床使用时间上限的2倍。
在动物试验中宜设置足够的、不同的观察时间点,观察特定时间点的评价指标,评估产品对实验动物的影响。在研究方案中宜充分说明不同观察时间点设置的合理性。观察时间点建议至少包含试验动物基线、ECMO启动后及ECMO治疗完成时,而在ECMO治疗过程中制定具体的观察时间点还需要结合试验设计、整体观察时间长短、评价指标等因素进行综合考虑,例如,在急性反应期(例如前2天或3天)可每间隔2-6个小时观察相关指标变化,进入稳定期后,可每隔12-24小时设置观察时间点。指标观察的时间间隔可根据观察指标的不同调整,比如,即便进入稳定期后,对于ACT、血气等仍可每6小时监测一次等。
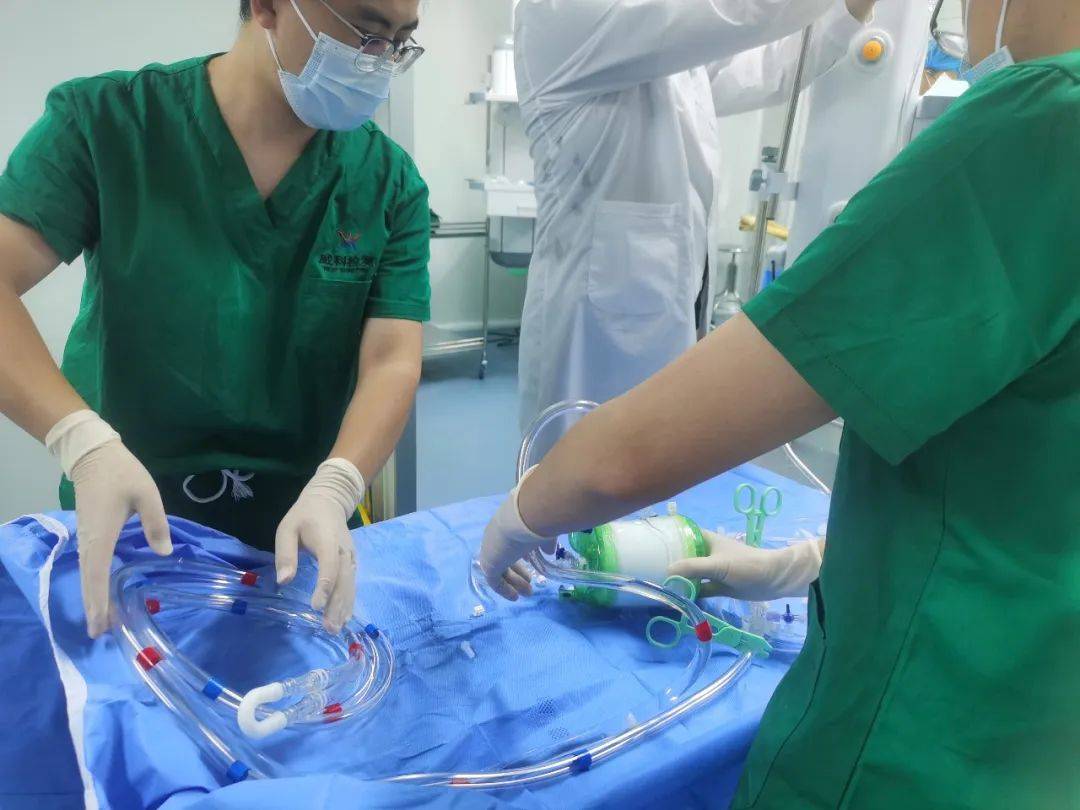
其他应注意的问题
ECMO循环套包产品动物试验研究过程中的实施、质量保证、实验动物管理等需要遵循《医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证》及相关动物试验研究的通用要求(如GB/T 35823等)。除此之外,还需要注意以下问题。
(一)试验机构
为保证动物试验结果真实、可靠,应使用质量合格的实验动物或检疫合格的实验用动物。申请人需与动物试验实施单位签订合同并共同设计、制订动物试验方案,上述资料作为产品质量体系管理文件存档。注册时提交申请人与动物试验实施单位共同确认并签章的动物试验报告。
(二)试验人员及质量保证
为保证动物试验的研究质量,应尽量避免不同操作者操作差异、动物麻醉死亡、操作死亡、操作后感染及其他意外情况对产品评价产生影响。建议申请人邀请有经验且经过培训的专业人员进行动物试验操作指导及评价。对所使用的生理监护仪、麻醉机和实验室血样检测设备等进行预防性维护。若采用外部实验室和病理学服务时应确保其质量控制的符合性。申请人需保存详细的试验情况记录及分析资料,包括以下适用的内容:所有试验用产品的信息、动物饲养及护理记录、镇痛麻醉记录、操作过程记录、抗凝方案记录、合并用药记录、器械治疗参数记录、原始病理照片等试验原始资料、治疗过程中产品组件更换记录及分析资料、对动物麻醉或操作死亡等非预期事件的有关证据及分析资料等。为了保证数据的溯源性,上述资料需作为产品质量管理体系文件存档。
(三)实验动物饲养环境、食物及护理
需根据所选实验用动物模型特点及试验目的等因素,充分考虑动物饲养环境、营养、动物作息、麻醉方法、操作技巧等,尽可能减少上述因素对试验结论造成的影响。所有实验动物都应可以自由获取一定数量的适于维持动物健康和体重的食物。确保实验动物摄入满足条件的规定量的食物、水等,以及符合标准的喂养操作程序。
在实验动物的护理中,需考虑适当的温度调节、电解质和热量平衡等因素以保证其生理稳态。所有操作均使用标准的无菌外科手术技术,力求将感染风险降到最低。考虑到血流动力学稳定性是ECMO治疗评价的一项主要标准,应避免清醒状态下动物受惊吓、异常身体活动等可能干扰血流动力学监测指标准确性的情况。可在试验前对动物进行驯化,使其提前适应试验环境。
在动物体内使用的测试和辅助设备等,需和人体内使用设备及其放置方式相同。例如,VV-ECMO可使用双腔静脉插管,置入动物右颈静脉至上腔静脉,或使用单腔静脉插管及动脉插管,分别置入动物右颈静脉和左颈静脉;VA-ECMO可使用单腔静脉插管及动脉插管,分别置入动物右颈静脉和右颈动脉。应根据动物的体重及血管条件采用相应的插管型号,相关参数的设定尽量标准化,符合ECMO指南或实践,根据动物的氧合情况动态调整参数设定。
若ECMO治疗在清醒状态的动物中进行,应保证有充分的时间和充足的人员来监测动物。动物从麻醉中恢复后,建议进行神经系统功能评价并记录。同时关注动物的疼痛表现,如磨牙、不安等,并及时调整药物控制其操作后疼痛。若出现四肢神经系统功能障碍,用止痛药或其他疼痛干预措施无法控制的动物疼痛,需要警惕血栓形成。试验期间对插管切口部位进行标准化护理,予以定期检查和清洁。试验期间,需对实验动物的整体健康状态(如精神状态、步态/姿势、饮食及排便情况、体重等)进行监测、评估和记录,而不仅限于试验评价指标。
申请人需要严格控制动物ACT水平,并给出其控制水平设定依据,动物抗凝方案建议参考人类ECMO期间临床抗凝方案和要求,并考虑动物本身特性,例如羊的ACT水平,建议常规控制水平不超过220s,并可增加APTT监测值作为参考。
鉴于血栓形成与产品运行过程中血流速度相关,特别是低流速下更容易形成血栓,因此建议动物试验过程中设定观察一定时长的低流速运行,例如可通过单独设立低流量组动物,或在研究组中低流量运行足够的时长。对于低流量组流速设定,建议根据产品实际最大流量宣称及产品设计等特点确定,并给出确定依据。例如,对于宣称最大流量7L/min的产品,原则上低流量组流速不宜超过2L/min。
(四)受试器械的搭建
若拟申报产品包括多种型号,申请人应根据动物试验的目的选择典型性的型号,并给出选择依据。动物试验中受试器械的操作方法,宜同预期的临床操作方法一致。如采用不同的操作方法,应确认未对试验结果及结论产生影响。
考虑到不同公司组件在使用参数、配合要求等方面影响因素以及评估便利性,采用套包形式注册并进行相关研究,可能更易于评价。若试验过程中,有多种不同器械参与动物试验观察,如循环回路中含受试器械管路,受试器械氧合器时,应分别描述受试器械,搭建方式及观察指标。申请人应在研究方案中对使用的受试器械进行详细描述,包括名称、结构及组成(含配合使用的附件、产品图示)、型号规格、批号、保存期限、保存条件、单个动物使用数量、使用频次(如适用)、是否重复使用等信息。宜建立受试器械接收、保管、使用记录、处理文件,保证样品使用具有可追溯性。
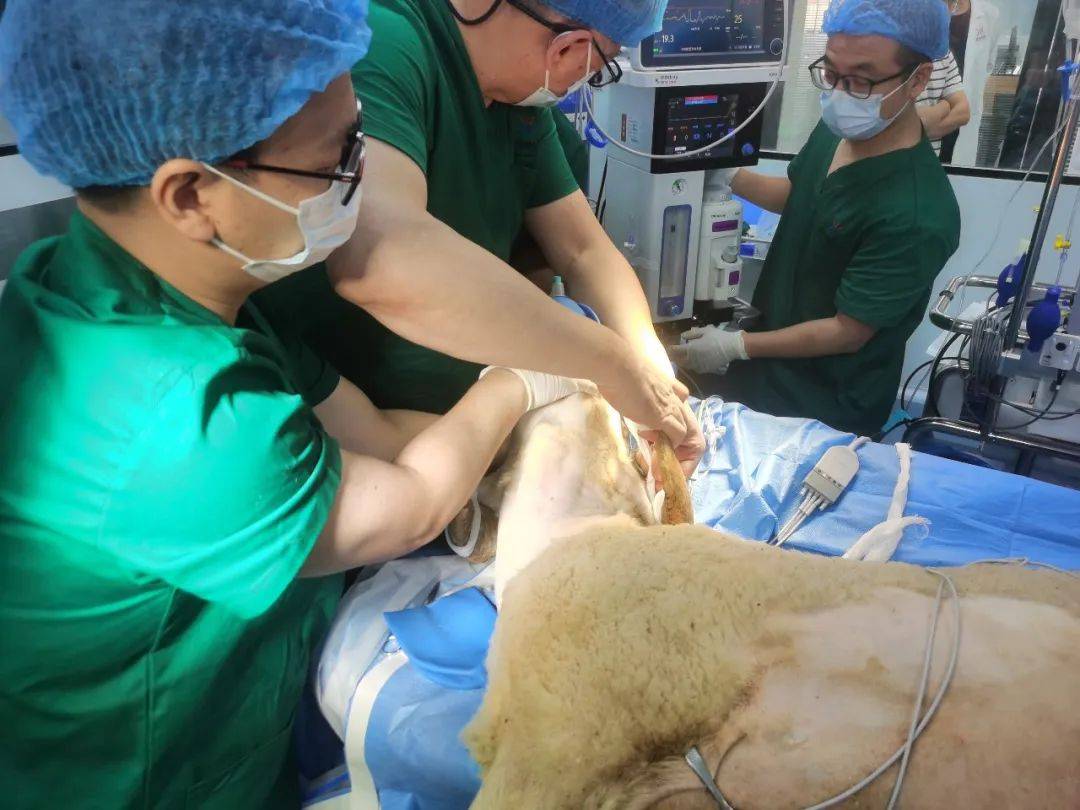

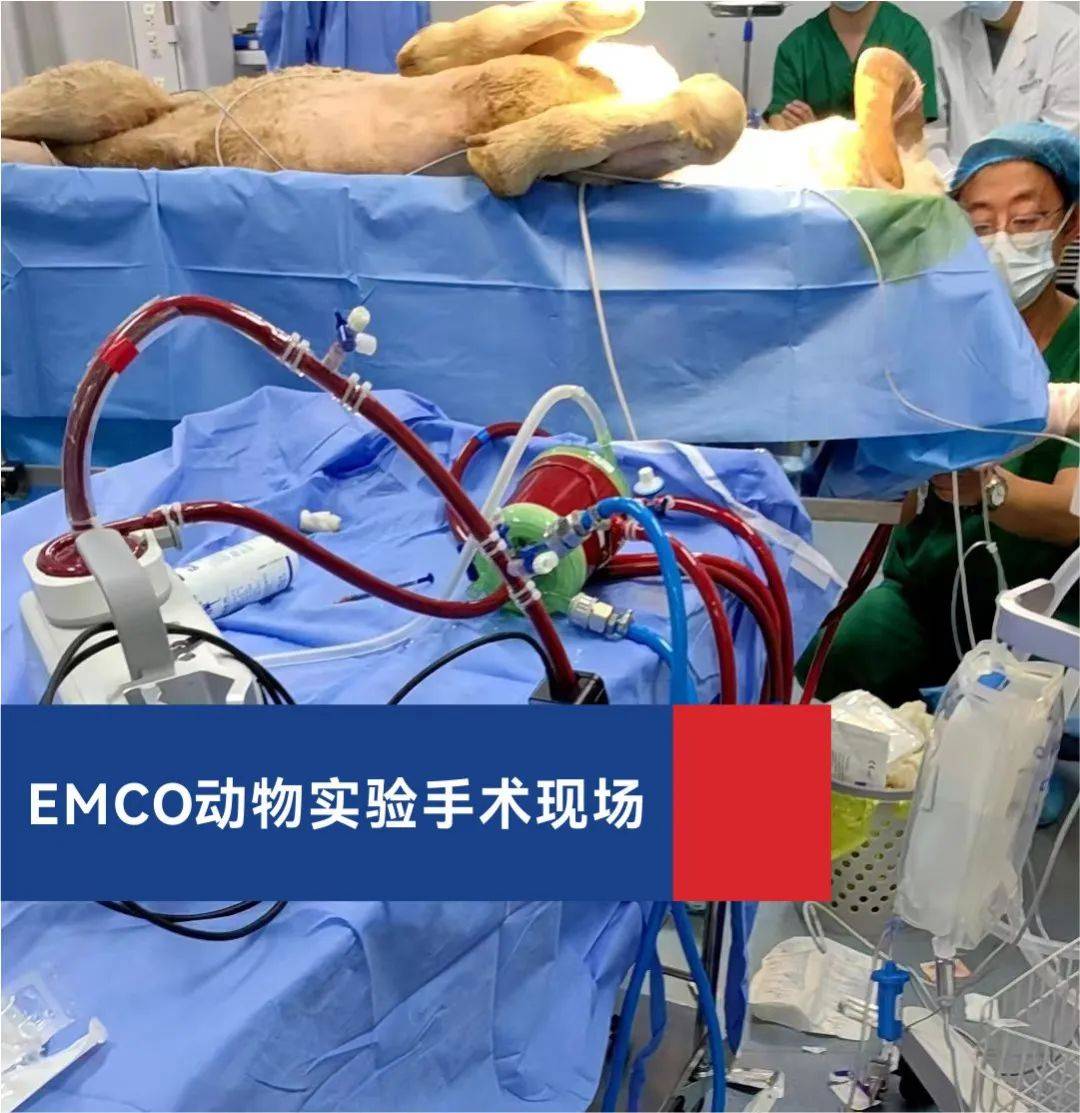
我们的服务覆盖无源医疗器械和有源医疗器械
无源医疗器械:高值介入医用耗材、整形/医疗美容产品、医用辅料、骨科植入物、齿科材料、体外循环器械、辅助生殖器械、医用防护器械、再生医学材料、组织工程材料。例如:一次性使用静脉留置针、医用缝合线、创面敷料、牙科种植体、血管支架、骨板、骨钉等。项目:生物学评价、临床大动物实验、化学表征、理化试验、EO残留量、老化试验、 微生物试验、包装运输验证等。
有源疗器械:医用电气设备,测量、控制和实验室用的电设备,体外诊断(IVD)医疗设备,医疗器械软件、医用电子产品、康复训练设备、电疗产品、热辐射产品、光辐射产品、磁疗产品、供氧设备、高频产品等,例如: 监护仪,心电图机,脑电图机,生化分析仪、医用分子筛制氧设备,神经和肌肉刺激器,高频电灼治疗仪,输液泵/注射泵,光治疗仪,红外治疗设备,雾化器,康复训练床,医疗器械软件测评等。项目:安规、环境试验和EMC检测、清洗灭菌验证、植入物疲劳性能验证、生物力学分析等。
-
 团建活动 | 澳门太阳集团城9728五周年庆暨“2023年度团建活动”精彩回顾2024-01-02
团建活动 | 澳门太阳集团城9728五周年庆暨“2023年度团建活动”精彩回顾2024-01-02 -
 《重组胶原蛋白医用敷料体外透皮吸收评价指南(荧光标记法)》团体标准发布实施2024-01-02
《重组胶原蛋白医用敷料体外透皮吸收评价指南(荧光标记法)》团体标准发布实施2024-01-02 -
 澳门太阳集团城9728苏州2023《第一届医疗器械质量与研发大会》圆满结束!2023-12-25
澳门太阳集团城9728苏州2023《第一届医疗器械质量与研发大会》圆满结束!2023-12-25 -
 澳门太阳集团城9728亮相深圳第88届中国国际医疗器械博览会(CMEF)展会2023-12-11
澳门太阳集团城9728亮相深圳第88届中国国际医疗器械博览会(CMEF)展会2023-12-11 -
 澳门太阳集团城9728·下川岛团建之旅|团结拼搏 共创未来2022-08-27
澳门太阳集团城9728·下川岛团建之旅|团结拼搏 共创未来2022-08-27 -
 热烈庆祝我司顺利取得CNAS认可资质2022-06-02
热烈庆祝我司顺利取得CNAS认可资质2022-06-02 -
 广东澳门太阳集团城9728实验动物使用许可证申请顺利通过省科技厅现场评2020-05-28
广东澳门太阳集团城9728实验动物使用许可证申请顺利通过省科技厅现场评2020-05-28
- 没有了
- 没有了